肿瘤细胞独特的代谢特征使其在氧气充足的条件下也倾向于依赖糖酵解提供能量,这一过程产生大量的乳酸在肿瘤细胞积累,并导致细胞内酸化。为应对这种酸中毒威胁,肿瘤细胞通过高表达单羧酸转运蛋白(MCT1和MCT4)持续将乳酸运输到胞外,从而维持细胞内pH稳态。而排出的乳酸导致了肿瘤微环境(TME)的酸化,这种酸性TME抑制细胞毒性T细胞(CTL)和自然杀伤(NK)细胞等免疫细胞的活性,同时促进调节性T细胞(Treg)和肿瘤相关巨噬细胞的免疫抑制功能。因此,通过抑制肿瘤细胞持续的乳酸输出,破坏其建立的细胞内/外pH平衡,能够有效抑制肿瘤的增殖、转移和免疫逃逸。
哈尔滨工业大学生命科学与技术学院杨奎琨教授团队在ACS Nano发表题为“A Biomimetic Microparticle Disrupting the Intracellular/Extracellular pH Homeostasis of Tumor Cells for Cancer Chemo-immunotherapy”的论文,介绍了一种工程化的肿瘤细胞来源的微粒(Syr/Dox-EMCH@MP),通过共同递送昔洛舍平(Syr)和低pH响应的阿霉素前药(Dox-EMCH),实现对肿瘤细胞内/外pH稳态的双重调控,从而启动级联的化学免疫治疗。第一作者左立萍,通讯作者杨奎琨教授。
该研究利用肿瘤细胞微粒(MP)作为载体,同时将MCT1和MCT4抑制剂Syr和Dox-EMCH装载到MP中。系统给药后,Syr/Dox-EMCH@MP可以特异性地靶向肿瘤组织并被肿瘤细胞摄取,其中Syr能有效抑制MCT1和MCT4活性,阻断乳酸外排,导致胞内乳酸累积和酸化加剧。这种细胞内的pH紊乱不仅能够直接诱导肿瘤细胞凋亡,而且激活了Dox-EMCH,引发强烈的免疫原性细胞死亡(ICD)。此外,肿瘤细胞乳酸外排的阻断通过减轻酸性TME逆转了免疫抑制(图1)。结果表明,Syr/Dox-EMCH@MP不仅能有效抑制原发肿瘤和远端肿瘤的生长,还能引发长效的免疫记忆,有效防止肿瘤转移。这项研究为通过系统性调控肿瘤细胞内/外pH稳态来实现高效的肿瘤治疗提供了新的思路。
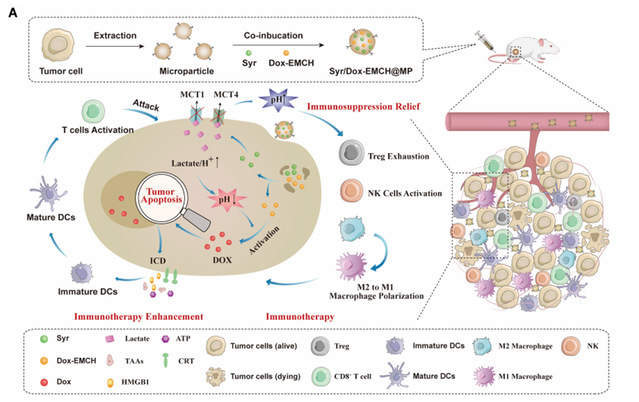
图1. Syr/Dox-EMCH@MP破坏肿瘤细胞内/外pH稳态实现化学免疫协同治疗示意图
论文链接:A Biomimetic Microparticle Disrupting the Intracellular/Extracellular pH Homeostasis of Tumor Cells for Cancer Chemo-Immunotherapy
https://doi.org/10.1021/acsnano.5c22145




 邮箱:life@hit.edu.cn
邮箱:life@hit.edu.cn 电话:0451-86403827
电话:0451-86403827 地点:哈尔滨市南岗区一匡街2号哈工大科学园2E栋
地点:哈尔滨市南岗区一匡街2号哈工大科学园2E栋