2026年2月26日,哈尔滨工业大学生命科学中心高明辉课题组在硫氧还蛋白还原酶1(TrxR1)促进肿瘤细胞铁死亡的分子机制研究中取得重要进展。相关成果以Selenoprotein Thioredoxin Reductase 1 Promotes Cancer Cells Ferroptosis by Suppressing GPX4 Expression为题发表在国际期刊Cell Death & Differentiation。该研究鉴定了TrxR1通过TrxR1-CRL4ACRBN-KEAP1-NRF2-GPX4轴促进铁死亡的新机制,并基于此为诱导肿瘤细胞铁死亡治疗方案提供了新思路。
铁死亡在人类癌症中发挥着至关重要的作用,作为一种肿瘤抑制过程,诱导肿瘤细胞发生铁死亡可能有利于肿瘤的治疗。铁死亡的生化本质是细胞内脂质过氧化物的过量累积,大量脂质活性氧的生成是其触发因素,而对脂质过氧化物的清除则起到铁死亡防御作用,这与细胞内的抗氧化系统密切相关。
在细胞主要的氧化还原调控体系中,谷胱甘肽(GSH‑GPx)与硫氧还蛋白(Trx‑TrxR)作为典型的巯基依赖型通路,发挥着核心、精细且广谱的氧化还原调控功能。GSH‑GPx系统中的谷胱甘肽过氧化物酶4(GPX4)作为目前已知的唯一一种广泛存在且能够还原有毒脂质氢过氧化物(LOOHs)的酶,其在铁死亡防御中的核心作用已被确立。而Trx-TrxR系统在铁死亡中的调控作用仍未得到充分阐明,其具体分子机制、功能意义以及与经典铁死亡通路间的交互关系尚不明确。
团队成员验证了前期通过pooled lentiviral RNA文库筛选出的Trx-TrxR核心组分硫氧还蛋白还原酶1(TrxR1)为铁死亡的正向调节因子,这颠覆了TrxR1作为经典抗氧化分子发挥保护性作用的传统认识:具有完整硒代半胱氨酸活性中心的TrxR1可以通过抑制GPX4的表达从而促进铁死亡的发生,而GPX4的缺失亦可促进TrxR1二聚体(TrxR1的功能活性形式)的形成。传统观点中,这两大抗氧化系统合二为一,共同清除活性氧胁迫信号;而在铁死亡中如同太极,互为阴阳,相互拮抗。
在机制上,这项研究验证了TrxR1-CRL4ACRBN-KEAP1-NRF2-GPX4这一全新铁死亡调控通路:研究关注了TrxR1引起的氧化应激传感器KEAP1(细胞内NRF2的主要抑制因子)的表达变化,首次鉴定了CRL4ACRBN E3泛素连接酶为KEAP1的特异性泛素连接酶(E3泛素连接酶是泛素化修饰的 “特异性决定者”),其中CRL4A为骨架蛋白,CRBN为底物衔接蛋白。另外,本研究阐明KEAP1的K84和K312为其泛素化的关键位点,解析了TrxR1通过抑制CRL4ACRBNE3复合体介导KEAP1泛素化,增强KEAP1的稳定性,进而NRF2(调控细胞内氧化还原稳态的核心转录因子)与KEAP1之间的相互作用增加,从而促进 NRF2 的泛素化及后续降解的机制。这一级联反应最终导致NRF2的下游靶点GPX4表达下调,进而增强肿瘤细胞对铁死亡敏感。
此外,临床数据表明与癌旁组织相比,TrxR1在多种癌症患者的肿瘤组织中表达上调,且与患者不良预后相关,提示TrxR1可作为铁死亡诱导肿瘤治疗的潜在生物标志物,为筛选适合铁死亡诱导治疗的肿瘤患者提供了新的检测靶点;另外,CRBN抑制剂沙利度胺与铁死亡诱导剂IKE联用可增强小鼠异种移植瘤的治疗效果。
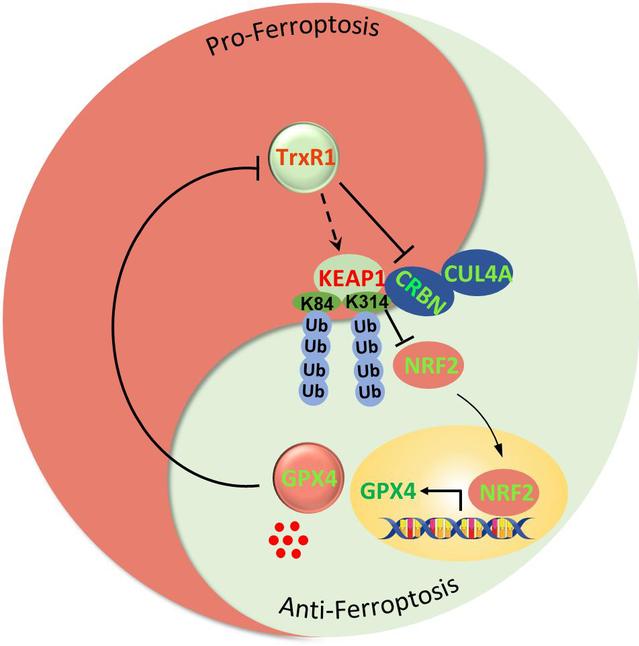
综上,本研究明确了TrxR1促进铁死亡的功能及具体机制,为靶向铁死亡的肿瘤精准治疗以及联合治疗方案的开发奠定了理论与实验基础。
哈尔滨工业大学生命科学中心高明辉研究员及威尔康奈尔医学院Zhang Wei为本文共同通讯作者。哈工大博士研究生栾静为论文第一作者。黑龙江中医药大学附属第一医院检验科、黑龙江中医药大学基础医学院武丹彤,哈工大何元正研究员及课题组博士段亚宁,高明辉团队其他成员参与其中。
本研究得到了国家自然科学基金、黑龙江省自然科学基金、黑龙江省春雁项目以及哈尔滨工业大学基金的支持。
原文链接:https://www.nature.com/articles/s41418-026-01691-z




 邮箱:life@hit.edu.cn
邮箱:life@hit.edu.cn 电话:0451-86403827
电话:0451-86403827 地点:哈尔滨市南岗区一匡街2号哈工大科学园2E栋
地点:哈尔滨市南岗区一匡街2号哈工大科学园2E栋